Recherche translationnelle en santé,
technologie pour la santé et recherche clinique
DEVIN / Axe 1 : Développement de biomarqueurs en IRM
Projets
Développement et validation d’une IRM multimodale du tronc cérébral pour explorer la microstructure tissulaire (DEVINET)
Financement: ANR PRC -2020 CES17 / Recherche translationnelle en santé
Début: Février 2021 / Durée: 4 ans
Coordinateur : P. Péran
Membres DEVIN impliqués dans le projet: J.A. Lotterie, F. Bonneville, G. Arribarat, A De barros, Levardon M, G. Mogicato, A Deviers, O Rascol, S. Silva, X. De Boissezon
Membre du plateau technique IRM 3T: Hélène Gros-Dagnac
Partenaire 2: Pr. Jean-Philippe Ranjeva / CRMBM /AMU-CNRS,(Marseille)
Partenaire 3: Olivier Andreoletti / École Nationale Vétérinaire de Toulouse (ENVT-INRAE)
Partenaire 4 : Pr. Olivier Rascol / Centre Hospitalo-universitaire de Toulouse (Toulouse)
Partenaire 5: Pr. Wassilios Meissner / Centre Hospitalo-universitaire de Bordeaux (Bordeaux)
Résumé: Le tronc cérébral humain, structure cérébrale complexe, est le principal centre relais pour les connexions afférentes et efférentes entre le cortex cérébral, le cervelet et la moelle épinière. Du fait de sa localisation spatiale, de sa taille et de ses caractéristiques tissulaires, le tronc cérébral pose des difficultés particulières en IRM. Ce projet est conçu pour définir une méthode pour les scanners de routine clinique. L’originalité de notre proposition est de développer un protocole tronc cérébral combinant acquisition et traitement de données. Nous avons identifié 3 défis à surmonter : 1) développer des séquences harmonisées IRM multimodales dédiées au tronc cérébral à haute résolution spatiale 2) déterminer les relations entre paramètres IRM et tissulaires 3) développer un outil libre multi-imagerie dédié au tronc cérébral. Enfin les outils développés seront validés en étudiant des patients présentant des dommages du tronc cérébral, afin de confirmer leur pertinence clinique.
—
Analyse des données de neuroimagerie: vers une approche intégrative
F. Nemmi, G.M. Mattia, P. Péran
Collaboration : X. Franceries, E. Villain et M.V. Le Lann
Objectifs:
L’objectif de cette thématique sera de définir une méthode de traitement de données où les signatures spatiales des marqueurs émergent d’une analyse sur l’ensemble des voxels du cerveau. Le développement d’un cadre généralisé unifié pour la combinaison de toutes les informations multimodales est une entreprise ambitieuse.
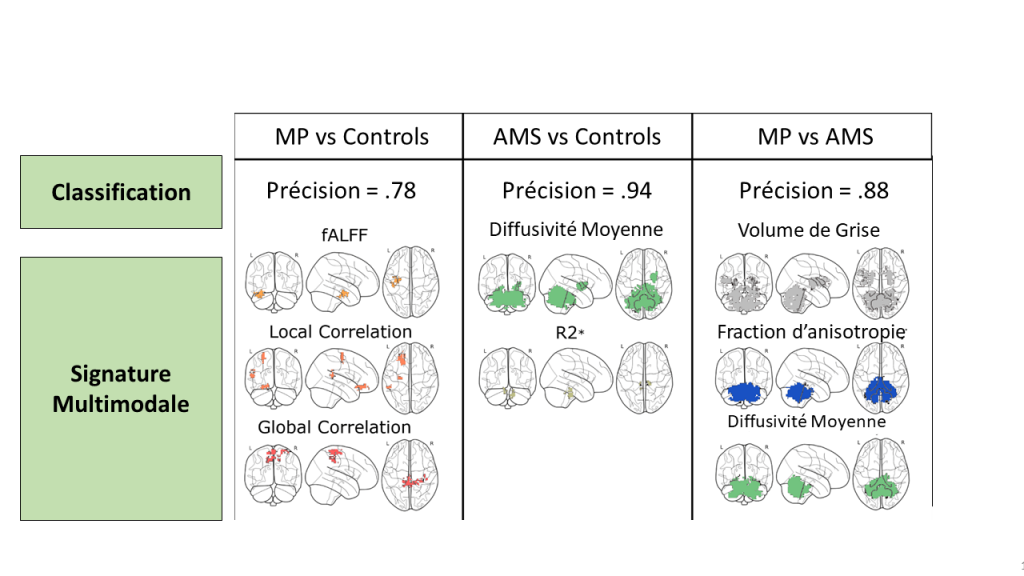
Un premier pas a été réalisé dans cette direction au travers d’une étude utilisant une nouvelle approche d’analyse des données IRMm structuro-fonctionnelle automatique, basée sur le voxel, utilisant une méthode de « support vector machine » (voir ci-dessous) .
—
L’aspect multidimensionnel intrinsèque à l’IRMm reste une problématique récurrente dans l’analyse des données de ce type d’approche. L’analyse de ces données par une approche de type réseaux de neurones (RdN) pourrait surpasser les limites des approches précédentes. Cependant, les RdN nécessite une grande quantité de données alors que les données de neuroimagerie sont de l’ordre de quelques dizaines patients au mieux de l’ordre de la centaine. L’objectif de ce travail sera de mettre en place une méthode d’analyse par réseaux de neurones des données multimodales de l’IRM afin (i) de classer des sujets sains en fonction de l’âge (ii) de discriminer les patients atteints de syndrome parkinsonien mais présentant des pathologies neurodégénératives différentes. Nous comparerons les résultats entre une méthode RdN et une méthode SVM (méthode déjà développée) en termes d’efficacité à classer et/ou discriminer les patients sur la base des mêmes cartes multiparamétriques (premier article soumis). Enfin, nous tenterons de trouver des solutions afin d’extraire des informations concernant le type de marqueurs IRM et le type de localisation anatomique pour l’architecture RdN la plus discriminante. En d’autres termes, peut-on extraire une signature spatiale multiparamétrique discriminante d’une analyse RdN ?
Travaux antérieurs
IRM multimodale structuro-fonctionnelle
Nous avons développé des approches multimodales structuro-fonctionnelles permettant d’appréhender la complémentarité entre les indices fonctionnels et structurels.
IRM multimodale structuro-fonctionnelle et apprentissage automatique
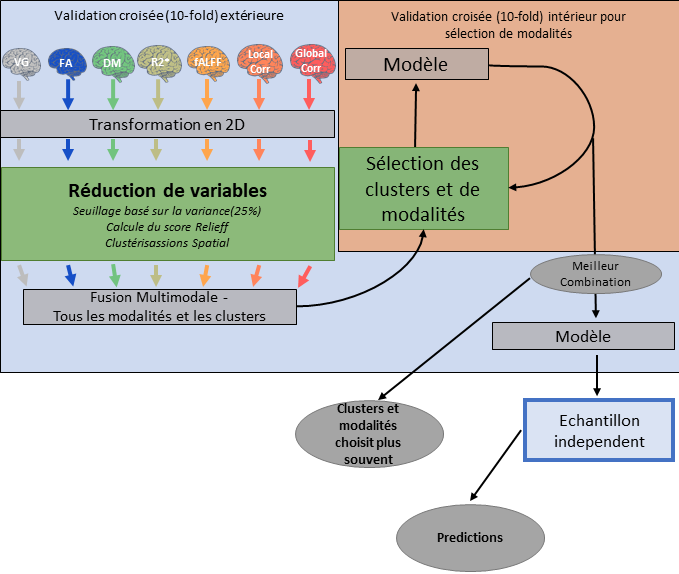
Pour exploiter au mieux les données d’IRM multimodale nous avons développé une pipeline d’analyse qui, à l’appui de techniques de sélections et réductions de variables et d’apprentissage automatique, est capable de discriminer entre une population pathologique et des sujets témoins ou entre deux populations pathologiques différentes. Cette discrimination est associée à ce qu’on appelle une signature multimodale : l’ensemble de régions cérébrale pour les différentes modalités d’imagerie que mieux différentie entre les populations.
- Validation en utilisent un modèle de pathologie génétique chez des enfants (Neurofibromatose) (Nemmi F et al., Human Brain Map; 2019)
- Application aux syndromes parkinsoniens (Maladie de Parkinson ; Atrophie Multisystématisée) (Nemmi F. et al., Neuroimage Clin ; 2019)
Connectivité fonctionnelle et connectivité structurelle (De Pasquale F., coll, Péran P., Hum Brain Mapp. 2017)
Une des problématiques actuelles des approches de connectivité fonctionnelle est de savoir si les dysconnexions observées sont purement fonctionnelles ou l’intégrité structurelle sous-jacente contribue à modifier la fonction. Afin de tenter de répondre à cette question, nous avons débuté un travail sur des sujets normaux sur la connectivité fonctionnelle et la connectivité anatomique. Un travail a été mené en collaboration avec un chercheur italien, Francesco de Pasquale.
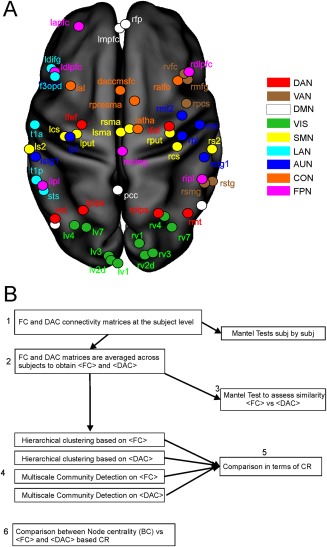
Une des problématiques actuelles des approches de connectivité fonctionnelle est de savoir si les dysconnexions observées sont purement fonctionnelles ou l’intégrité structurelle sous-jacente contribue à modifier la fonction. Afin de tenter de répondre à cette question, nous avons débuté un travail sur des sujets normaux sur la connectivité fonctionnelle et la connectivité anatomique. Un travail a été mené en collaboration avec un chercheur italien, Francesco de Pasquale.
Figure à gauche: Analyse de la connectivité structurelle et fonctionnelle
—
Approche IRM multimodale
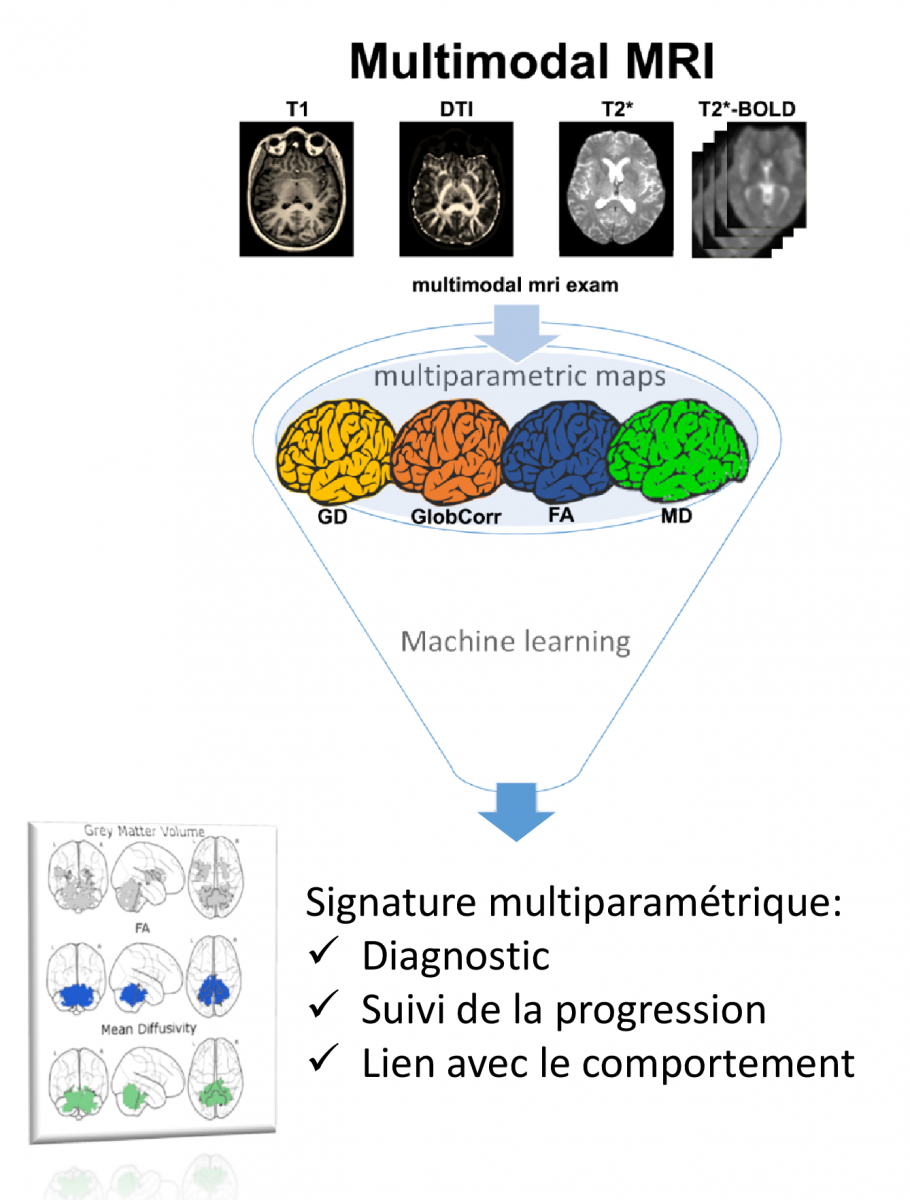
Nous avons développé une approche IRM combinant différents indices quantitatifs pouvant caractériser des types distincts et complémentaires de modifications physiopathologiques. Cette approche multiparamétrique vise à enrichir les données d’imagerie susceptibles d’améliorer le diagnostic et le pronostic au sein du spectre complexe des pathologies du cerveau.
Premières validations cliniques de l’approche IRM multimodale:
- IRM multimodal & Vieillissement normal (Cherubini A, Péran P, et al. Neuroimage. 2009)
- IRM multimodal & Maladie de Parkinson (Péran P, et al. Brain ,2010)
Principe de l’approche IRM multimodale
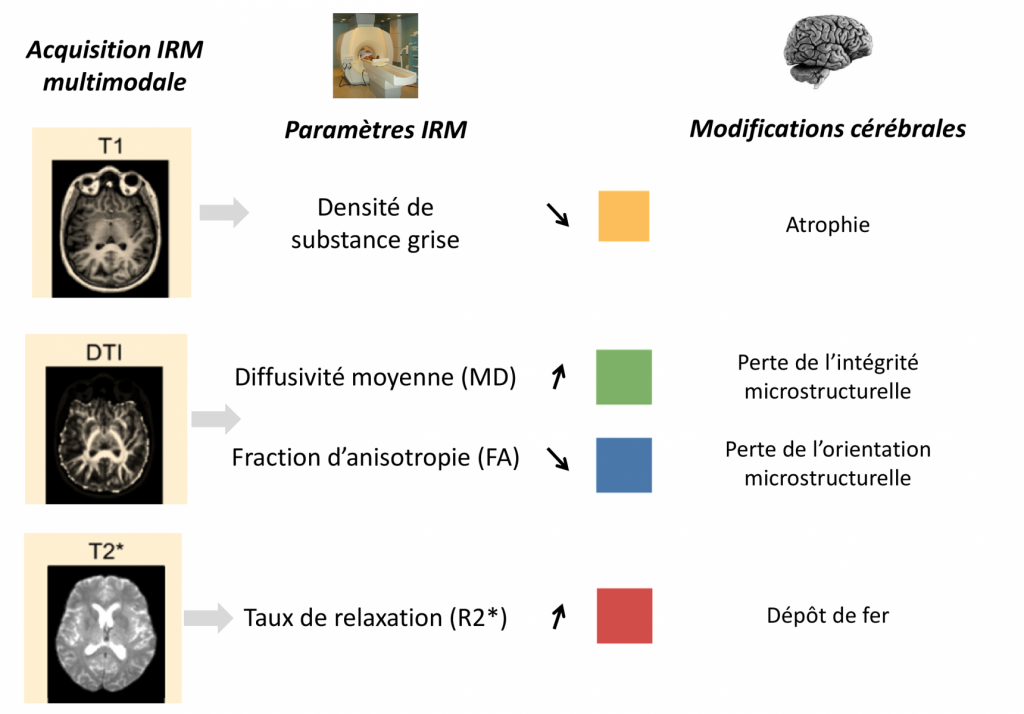
—
IRM: Quantification du fer intracérébral
La dysrégulation du métabolisme du fer et son accumulation dans différentes régions du cerveau sont impliquées dans la physiopathologie de nombreuses maladies neurodégénératives. Ainsi nous avons développé une méthode basée sur la relaxométrie T2* qui s’est avéréereproductible et sensible permettant d’évaluer le contenu de fer intracérébral in vivo:
- Mise au point et conception de l’approche (Péran P, et al. J Magn Reson Imaging. 2007)
- Validation indirecte de la mesure du fer intracérébral (Péran P, Hum Brain Mapp. 2009)
- Imagerie du fer et image de diffusion (Cherubini A, Péran P, et al. Magn Reson Med. 2009)
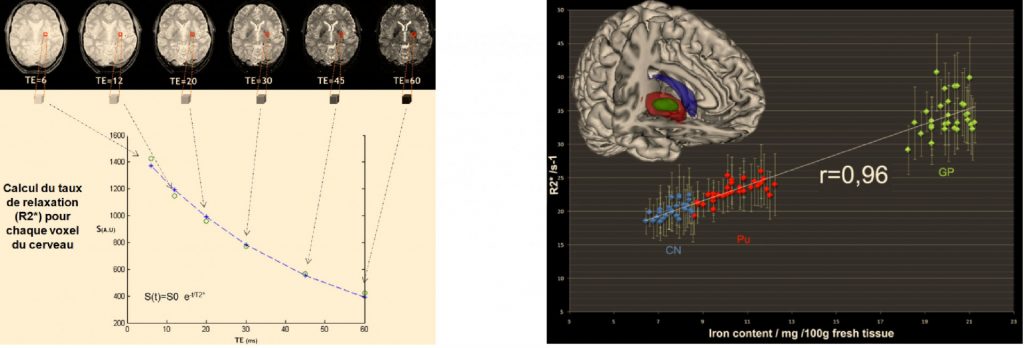
—
IRM fonctionnelle
Connectivité fonctionnelle chez les sujet sains (De Pasquale F., coll, Péran P., 2013)
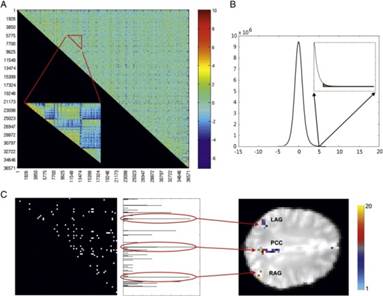
L’analyse des réseaux au repos en analysant la connectivité fonctionnelle des données d’IRMf au repos est une méthode qui permet d’extraire des indices fonctionnels du cerveau. Ainsi récemment de nombreuses études ont montré que la connectivité fonctionnelle cérébrale peut être un outil intéressant afin d’étudier l’intégrité fonctionnelle du cerveau dans de nombreuses pathologies. Nous avons développé, en collaboration avec le département de radiologie e l’IRCCS Santa Lucia (Rome, Italie), une approche « data-driven » du cerveau entier permettant d’extraire des nœuds fonctionnels lors d’une expérience IRMf de l’état de repos. Nous avons conduit une étude sur 20 sujets sains jeunes qui ont réalisé un examen IRMf au repos dans le département de radiologie de la Santa Lucia. Les résultats ont montré que deux principaux noyaux émergent significativement : le cortex cingulaire postérieur (PCC) et et l’aire motrice supplémentaire (SMA). Leurs cartes de connectivité fonctionnelle, seuillées à trois niveaux statistiques, ont révélé la présence de deux systèmes complexes. Un système est compatible avec le réseau par défaut (DMN) qui se raccorde progressivement à des régions visuelles, l’autre centré sur les régions à moteur qui se relie progressivement à des parties plus sensori-spécifiques de cortex. Ces deux réseaux à grande échelle convergent finalement vers des régions appartenant d la face médiale de la DMN, permettant potentiellement interactions inter-réseaux. Cette méthode a pour vocation d’être intégrée aux marqueurs structuraux de l’approche IRMm.
Acteurs de l’axe

Germain ARRIBARAT

Fabrice BONNEVILLE

Samuel BOUCHER

Benjamin CARTIAUX

Alexandre DA COSTA

Amaury DE BARROS

Sabrina HOUIDEF

Jean Albert LOTTERIE

Giulia Maria MATTIA

Giovanni MOGICATO

Charles MONTEL

Patrice PÉRAN