Recherche translationnelle en santé,
technologie pour la santé et recherche clinique
iDREAM / Axe 1 iDREAM : Imagerie de la réparation cérébrale motrice
Médecine régénérative: Implants cérébraux et thérapie cellulaire
L’axe est coordonné par Isabelle Loubinoux et Franck Desmoulin.
Objectifs scientifiques
Nous développons des thérapies qui s’adressent aux patients avec de lourds handicaps (AVC, Traumatisme crânien grâve).
Notre approche se base sur la régénération de la lésion cérébrale avec des implants et/ou des greffe de cellules.
L’imagerie IRM est un outil crucial pour effectuer un suivi longitudinal afin d’appréhender l’intégration des implants ou des cellules dans le cerveau, leur vascularisation, la dégradation des biomatériaux, leur innocuité, et leur sécurité, ainsi que la détection d’événements indésirables.
Les implants régénératifs
L’implant en silicone fonctionnalisé
La médecine régénérative apporte de nouveaux espoirs de traitement qui résident sur des neuro-implants (thérapie cellulaire sur biomatériaux) afin de rétablir des pontages longue-distance des aires cérébrales. L’équipe a fait la preuve de concept de neuro-implants améliorant la performance motrice chez le rongeur. La sécurité est démontrée chez le primate non-humain (marmouset).
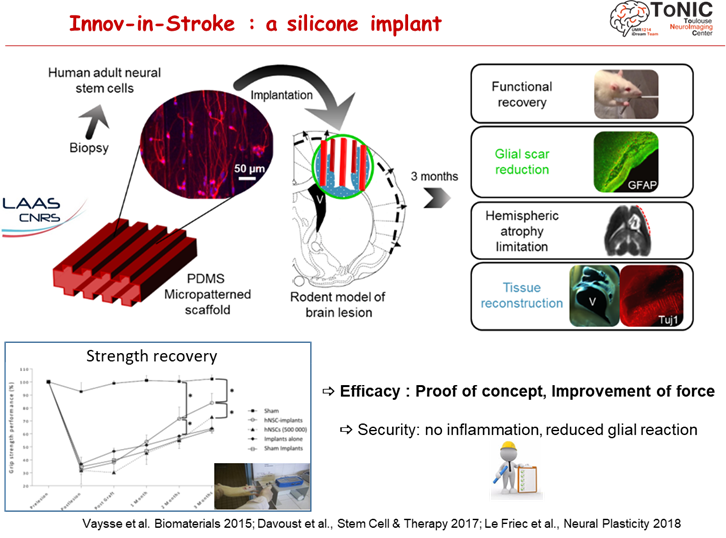
Un essai clinique de sécurité des implants est en préparation: projet FAVOUR (ANR Médécine Régénérative et programme Messidore) sur des patients traumatisés crâniens graves.
Collaboration CIC-IT de Bordeaux.
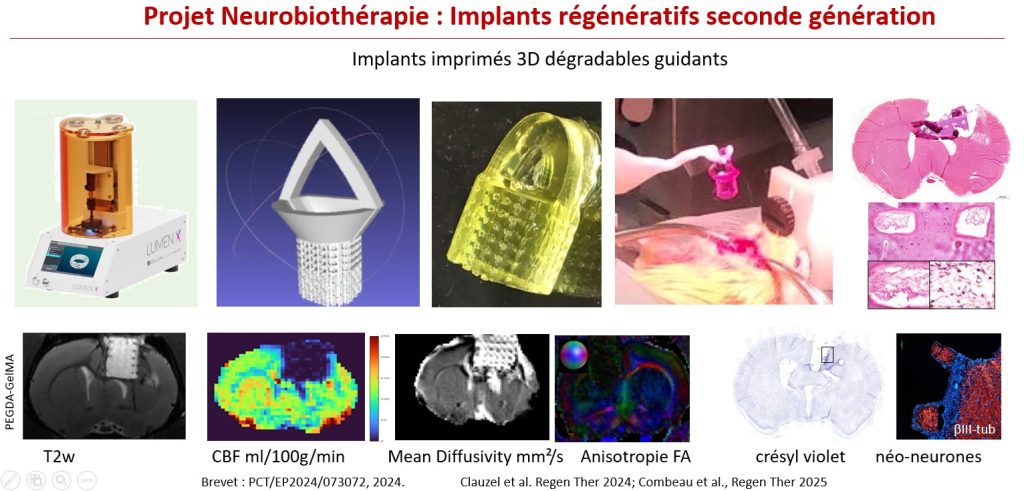
L’implant imprimé 3D dégradable
La seconde génération d’implants cérébraux régénératifs se focalise sur des implants dégradables. L’impression 3D leur confère une architecture complexe mimant le cortex cérébral en six couches interconnectées. L’imagerie T2 offre une bonne visualisation de l’hydrogel et de sa dégradation au cours du temps. L’imagerie de perfusion pCASL permet de suivre la revascularisation de l’implant. L’imagerie de tenseur de diffusion mesure la diffusivité de l’eau dans le matériau, les pores et le tissu (Projet Matrix, financement ANR ASTRID).
Collaborateurs: CEA-Tech Toulouse, Healshape, ICGM, ENVT LabHPEC.
La thérapie cellulaire
Thérapie cellulaire à partir de glie entérique pour la régénération cérébrale
Ce projet contribue aux études de réparation cérébrale dans un modèle préclinique de lésion cérébrale aiguë chez le rat. Les mécanismes actuels de plasticité cérébrale sont insuffisants pour une récupération fonctionnelle complète, et les interventions utilisant des cellules exogènes représentent une approche prometteuse.
Nous avons évalué une stratégie innovante pour la régénération du tissu nerveux, utilisant des cellules gliales adultes isolées du système nerveux entérique. Chez l’humain, ces cellules soutiennent les neurones, présentent une grande plasticité, et libèrent des facteurs neurotrophiques et des cytokines anti-inflammatoires.
L’objectif est de démontrer que les cellules gliales entériques humaines représentent une thérapie efficace après lésion cérébrale aiguë. Dans notre modèle, la régénération tissulaire endogène et la survie des cellules greffées ont été évaluées longitudinalement par IRM in vivo et post-mortem via analyses immunohistochimiques. La récupération motrice a été mesurée à l’aide de tests validés.
Enfin, nous proposons une administration peu invasive par voie intranasale, directement connectée au cerveau, offrant un fort potentiel translationnel.
Porteurs du projet : Nina Colitti (Post-doctorante, ToNIC), Carla Cirillo (CRCN Inserm, Imagine).
Collaborateurs : Isabelle Loubinoux (DR1), Franck Desmoulin (CRHC). Ingénieure d’étude: Alexa Gouardères.
Projet soutenu par la Fondation des Gueules Cassées et les Fonds pour la Recherche sur l’AVC.
.
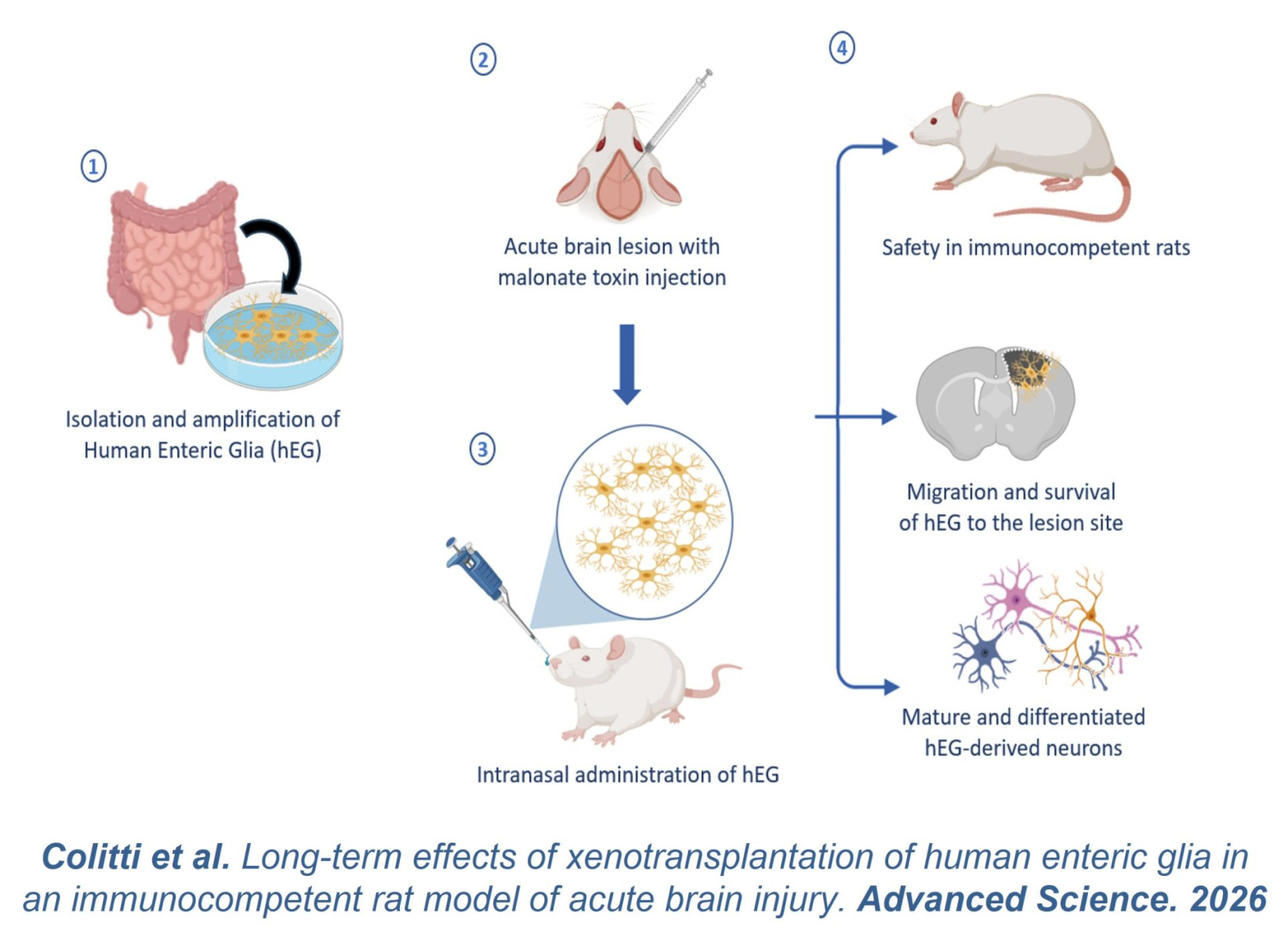
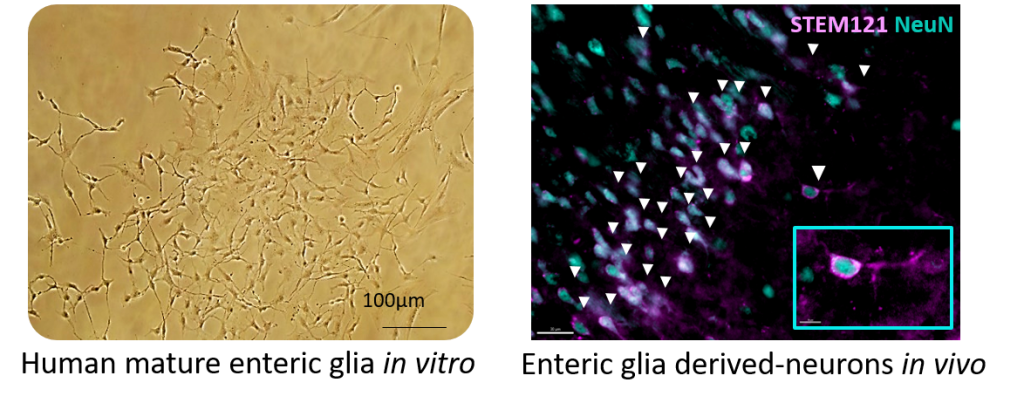
Des cellules gliales entériques humaines ont été greffées par voie intranasale dans des cerveaux de rats et se sont préférentiellement différentiées en neurones (Colitti et al. Adv Sci 2026).
Glie entérique et hydrogels 3D dans les lésions cérébrales acquises
Les thérapies cellulaires pour la régénération du cerveau sont actuellement limitées en termes de sécurité et d’efficacité. Les résultats obtenus au sein de notre équipe montrent le potentiel régénératif des cellules gliales entériques. Ce projet s’appuie sur le potentiel des ces cellules, utilisées seules ou en association avec des biomatériaux de type hydrogel, afin de créer un microenvironnement favorable à leur survie, leur intégration et à la modulation des processus de réparation cérébrale.
Nous testons les cellules gliales entériques avec un support 3D (hydrogel GalC9) pour améliorer la régénération des tissus après une lésion cérébrale. Notre proposition se distingue par les caractéristiques intrinsèques des cellules gliales entériques, offrant une stratégie sûre et potentiellement plus efficace par rapport aux approches existantes. Ceci a des implications cliniques et éthiques significatives, promettant des avancées dans le domaine de la régénération du cerveau.
Porteurs du projet : Carla Cirillo (CRCN Inserm, Institut Imagine), co-porteur : Juliette Fritemann (CRHC CNRS, Laboratoire SofMat)
Doctorante : Edwige Rice, ToNIC
Post-doctorante : Nina Colitti, ToNIC
Collaborateurs : Werend Boesmans (Professeur Associé, Hasselt University – Belgique) ; Franck Desmoulin (CRHC, ToNIC).
Projet soutenu par la Fondation des Gueules Cassées et le CDU de l’Université de Toulouse.
L’imagerie préclinique
Biomarqueur de dégénérescence secondaire
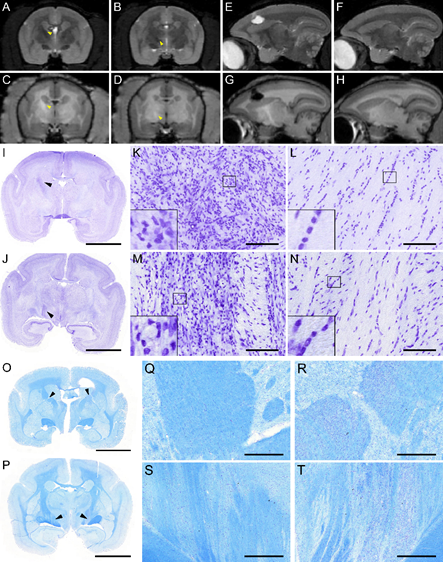
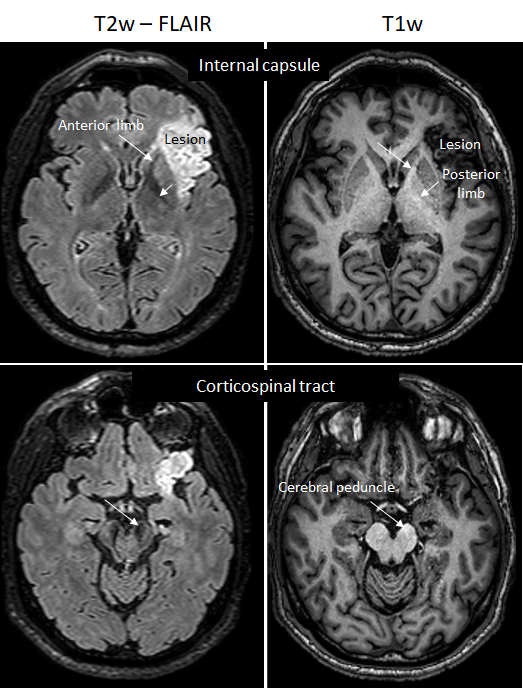
Nous avons découvert un nouveau biomarqueur de la gliose accompagnant la dégénérescence axonale chez le patient AVC et le primate non-humain cérébrolésé (marmouset). Plusieurs mois après la lésion corticale, le faisceau corticospinal subit une perte de myéline, une infiltration astrocytaire et une réaction microgliale. Elles induisent une perte d’intensité sur les IRM T2 et une légère hyperintensité sur les IRM T1 (Le Friec et al., Trans Stroke Res 2020).
Mise en évidence de la dégénérescence du faisceau corticospinal
Ouverture de la barrière hémato-encéphalique
Notre cerveau est protégé par la barrière hémato-encéphalique. Mais certains médicaments ne peuvent la traverser.
L’imagerie préclinique permet de mettre au point des procédures d’ouverture temporaire de la barrière hématoencéphalique et de déterminer les conditions sécuritaires.
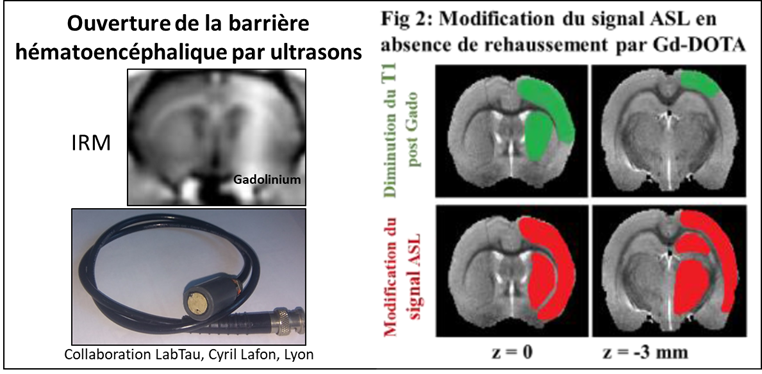
(Labriji et al. Magnetic Resonance in Medecine, 2023)