Recherche translationnelle en santé,
technologie pour la santé et recherche clinique
Axe 2 : Adaptation et réadaptation motrices – ADAPT! / Approche multidimensionnelle des cocontractions spastiques chez le sujet cérébrolésé

Mécanismes physiopathologiques, conséquences sur les altérations du mouvement du membre supérieur et implications thérapeutiques.
Cette thématique de recherche transactionnelle est centrée sur l’étude des substrats neuromusculaires de l’hyperactivité musculaire se manifestant lors des mouvements du membre supérieur chez le sujet cérébrolésé. Cette expression de l’hyperactivité musculaire correspond à des cocontractions spastiques. A travers une approche multimodale combinant cinématique 3D, électromyographie, électroencéphalographie et imagerie anatomique et fonctionnelle par IRM, l’objectif est de contribuer à une meilleure connaissance des mécanismes neuromusculaires impliqués dans cette expression de l’hyperactivité musculaire. L’impact des cocontractions spastiques sur les altérations du mouvement est également exploré, et des injections intramusculaires de toxine botulique dans les muscles hyperactifs sont utilisées en tant que paradigme expérimental permettant d’étudier la plasticité de ces phénomènes.
La meilleure compréhension de l’impact des cocontractions spastiques sur les altérations du mouvement permet de lever un verrou dans le développement d’une neuroprothèse d’assistance à la préhension dont l’objectif est de restaurer des capacités de préhension du membre parétique après un accident vasculaire cérébral.
Enfin, nous contribuons au développement d’outils d’évaluation de la performance factuelle du membre supérieur utilisables en situations écologiques de vie quotidienne.
Projets de recherche
Multidimensional evaluation of upper limb function in adult with stroke: Analysis of psychometric properties of clinical outcome measures and actual performance assessment – Thèse de Doctorat Claire VILLEPINTE (soutenue le 16/11/2021), sous la co-direction de David GASQ et Xavier de BOISSEZON.
Despite variation, Upper Limb Impairment (ULI) post-stroke typically includes: paresis, somatosensory deficit, as well as abnormal voluntary movement and muscle tone contralateral to brain lesion, defined as hemiparesis. Symptoms post-stroke vary; however neurological impairment leading to loss of arm function and/or reduced arm use is one of the most common deficits post-stroke. Empirical studies estimate 50 to 70 per cent of individuals in acute and 50 per cent in chronic phases have ULI.
ULI has a direct impact upon functional tasks impacting quality of life. Current literature demonstrates strong associations between UL performance level and functional independence contributing to disability and activity limitation.
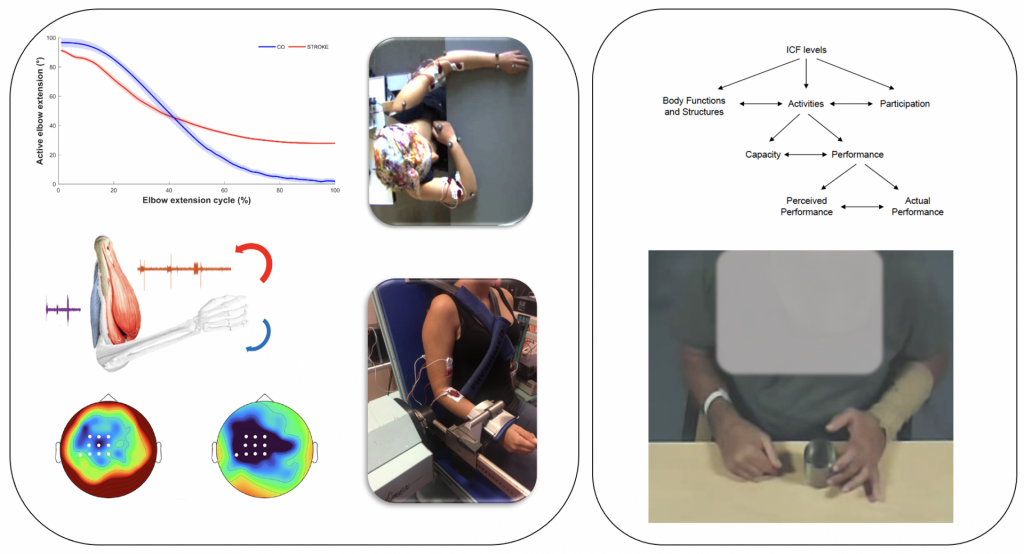
Due to the multi-faceted nature of UL function and performance, evaluation should be multidimensional including activity and participation limitations, congruent with shifts in clinical practice and research. Present in numerous systematic reviews, the International Classification of Function, Disability and Health framework (ICF) provides a conceptual framework ensuring multidimensional evaluation of UL function. Tendency of the use of combined outcome measure evaluation in relation to the ICF components is strong and findings highlight the consensus that no single measure encapsulates complete UL function. Therefore, grouped measures providing ecological indicators of function will contribute to comprehensive assessment.
There is a lack of validated and standardised outcome measures for the UL post-stroke for use in French physical rehabilitation practice and research-based trials guiding evidence-based practice. Currently, there are no measures that provide assessment of somatosensory capacity of the UL, nor are there established validations of measures of actual performance. This has lead to a lack of standardised administration protocols resulting in variation of scoring among professionals and structures, impacting upon the validity and reliability of assessment post-stroke. The Erasmus modified Nottingham Sensory Assessment (EmNSA) provides a standardised and validated assessment measure of somatosensory capacity post-stroke with potential uses in French practice. Regarding perceived performance, subjective semi-structured questionnaires, such as the Motor Log Activity (MAL) and the Arm Activity Measure (ArmA) provide valuable measures currently implemented to measure rehabilitation methods such as constraint induced therapy and botulinum toxin injection interventions. Current literature demonstrates a multitude of outcome measures of the UL; however systematic reviews demonstrate no clear recommendations exist regarding use of preferred tools. Synthesis of these measures also highlight overlapping of test items and repetition of the testing of ICF components. Comprehensive comparison of measures addressing psychometric qualities and identifying appropriateness for use across different clinical interventions can contribute to identification and selection of suited assessments reducing time and resources in clinical practice. Statistical methods with methods such as Rasch and Guttman analyses will also address repetition of test items and contribute to reduced testing times addressing psychometric qualities appropriate to rehabilitation research.
Caractérisation clinique et corrélats neuronaux anatomo-fonctionnels des cocontractions spastiques du membre supérieur après un accident vasculaire cérébral – Thèse de Doctorat Camille CORMIER, sous la co-direction de David GASQ et Isabelle LOUBINOUX.
Le déficit d’extension active du coude, souvent présenté par les patients hémiplégiques, impacte directement les capacités de préhension en altérant la phase d’approche. Il est lié à la parésie des muscles agonistes et à l’hypertonie spastique des muscles antagonistes fléchisseurs, et notamment à la cocontraction spastique. Cette dernière correspond à un renforcement de la coactivation des muscles antagonistes présente de manière physiologique au cours du mouvement volontaire. Les cibles du traitement de l’hypertonie spastique par injection de toxine botulinique sont souvent déterminées par l’évaluation de la spasticité, alors que notre équipe a montré que les altérations du mouvement sont plutôt liées à la présence de cocontractions spastiques qu’à la spasticité.
Nous souhaitons étudier un certain nombre de questions sans réponse claire dans la littérature actuelle : influence de la vitesse de réalisation du mouvement sur l’intensité des cocontractions spastiques et influence des composantes de résistance passives susceptibles de contribuer à l’altération du mouvement. Nous allons également étudier les corrélats neuronaux anatomo-fonctionnels des cocontractions spastiques à partir d’IRM anatomiques et de diffusion.
Pour ces travaux, nous exploiterons les données instrumentales et cliniques enregistrées pour les études ULISCC-STROKE (« Étude des cocontractions spastiques et limitation des mouvements actifs du membre supérieur avant et après injection de toxine botulique en soin courant chez des patients post-AVC » ; N° ID-RCB : 2017-A00579-44 ; Promoteur : CHU de Toulouse ; PI : David Gasq) et ULAFBoT-STROKE (« Effets de la toxine botulique et de la plasticité neuromusculaire induite sur la facilitation des mouvements du membre supérieur en post-AVC » ; N° ID-RCB : 2018-000941-38 ; Promoteur : CHU de Toulouse ; PI : David Gasq).
Etude neuro-biomécanique des mécanismes centraux du contrôle de la motricité volontaire saine et altérée : modifications induites par des injections de toxine botulique associées à de la rééducation chez le sujet post-AVC – Thèse de Doctorat Célia DELCAMP (soutenue le 03/07/2023), sous la co-direction de David AMARANTINI et David GASQ.
Ce projet de thèse pluridisciplinaire se situe au croisement des neurosciences, de la biomécanique, du contrôle moteur et du traitement du signal et a pour objectif, dans une double perspective fondamentale et clinique, de contribuer à une meilleure compréhension des mécanismes nerveux centraux de contrôle de la motricité saine et altérée. D’une manière originale, l’implication et la contribution de ces mécanismes nerveux d’origines spinale et supraspinale seront étudiées à travers l’analyse des cohérences cortico-musculaire (CMC) et intermusculaire (IMC), combinée à celle de l’activité corticale oscillatoire (ERD) chez des sujets sains et des sujets post accident vasculaire cérébral (post-AVC) traités par toxine botulique (TBA) et rééducation.
L’étude centrale de ce travail, pour laquelle un CPP a déjà été obtenu (ULAFBOT-Stroke « Effets de la toxine botulique et de la plasticité neuro-musculaire induite sur la facilitation des mouvements du membre supérieur en post-AVC » ; N° EudraCT : 2018-000941-38 ; promoteur : CHU de Toulouse ; PI : David Gasq ; début : juin 2020) portera donc sur des sujets volontaires sains (n=40) et des patients post-AVC chroniques (n=40). La toxine botulique étant largement prescrite en clinique afin d’améliorer la fonction motrice (Welmer et al., 2010), son effet inhibiteur sera étudié au regard de la performance motrice lors de mouvements actifs des membres supérieurs, sur les différents biomarqueurs des mécanismes de contrôle de la motricité des patients post-AVC comparativement à des sujets sains. L’étude de la plasticité du système neuromusculaire des patients sera effectuée à court terme suite à une injection de TBA ainsi qu’à long terme après trois injections répétées.
Du point de vue méthodologique, ce projet repose sur une approche particulièrement pertinente pour étudier de manière approfondie les mécanismes de contrôle de la motricité humaine (Boonstra, 2013), qui repose sur l’étude concomitante des grandeurs neurophysiologiques suivantes :
i) Les interactions cortico-musculaires quantifiées entre le cerveau et les muscles, par l’étude de la cohérence entre le signal électroencéphalographique (EEG) et électromyographique (EMG)
ii) Les interactions intermusculaires, par l’étude de la cohérence entre deux signaux EMG
iii) La réactivité de l’activité corticale oscillatoire (ERD) quantifiée à partir de l’EEG.
A visée fondamentale, nous confronterons les données de CMC à d’autres marqueurs afin d’améliorer les connaissances relatives à son rôle fonctionnel. Dans un même objectif, l’IMC sera confrontée à d’autres approches de synergies intermusculaires. Une IRM effectuée à l’entrée du protocole chez les patients nous permettra de caractériser les lésions afin d’étudier leur impact sur les différentes cohérences et sur l’activité corticale oscillatoire et d’améliorer la méthodologie de quantification de ces biomarqueurs. Cette approche expérimentale originale contribuera à apporter des connaissances nouvelles sur les mécanismes centraux impliqués dans le contrôle du mouvement sain et pathologique.
Ce travail vise aussi une valorisation clinique et translationnelle. En éclaircissant la compréhension des effets induits par le traitement sur les mécanismes de contrôle de la motricité altérée par l’AVC, ainsi que sur l’ensemble des structures aux niveaux périphérique, spinal et central du système neuromusculaire, cette étude permettra d’ajuster la cible et la temporalité des injections de TBA chez les patients post-AVC.
L’équipe constituée dispose de l’ensemble des matériels, compétences techniques et technologiques, autorisations éthiques et de lieux permettant de concrétiser ce projet dans les meilleures conditions, avec un niveau d’exigence requis dans le cadre d’un Contrat Doctoral Unique. L’implication de la candidate dans la mise en œuvre du protocole la rend d’ores et déjà autonome à la réalisation des expérimentations et à l’ensemble des traitements des données. L’excellence de son parcours universitaire et de ses activités de recherche attestent de sa maturité et de son dynamisme scientifique. Ces éléments, associés à sa capacité à déjà valoriser ses travaux, sont un gage de faisabilité et de réussite de ce projet de doctorat.
Conception et évaluation d’une neuroprothèse de préhension embarquée pour restaurer des capacités de préhension du côté parétique en vie quotidienne chez des personnes ayant une hémiplégie suite à un AVC – Thèse de Doctorat Ronan LE GUILLOU (soutenue le 18/12/2023), sous la co-direction Christine AZEVEDO-COSTE (équipe CAMIN INRIA, Montpellier) et David GASQ.
Suite aux déficiences motrices liées à un accident vasculaire cérébral, moins de 20% des patients utilisent la main affectée dans les tâches de la vie quotidienne. Sans solution thérapeutique à l’heure actuelle, il y a un réel besoin pour une neuroprothèse d’assistance à la préhension intuitive permettant d’effectuer des tâches bi-manuelles.
Afin de rendre possible l’utilisation d’un tel dispositif embarqué dans les tâches de la vie courante, des modalités de contrôle intuitives et robustes doivent être développées.
L’objectif est de concevoir et modéliser des méthodes de contrôle utilisant divers types d’entrées (EEG, EMG, voix, contacteur ou IMUs par exemple). Ces méthodes de contrôle devront rester intuitives afin d’améliorer l’acceptation, pouvoir être paramétrées pour faciliter l’utilisation en conditions réelles et posséder une détection de l’intention robuste afin de permettre une utilisation fonctionnelle dans les multiples tâches de préhension de la vie quotidienne. Ce projet est basé sur l’étude PREHENS-STROKE (« Évaluation de l’impact fonctionnel d’une neuroprothèse de préhension auto-pilotée chez le patient hémiparétique vasculaire » ; N° ID-RCB : 2020-A01660-39 ; Promoteur : CHU de Toulouse ; PI : David Gasq) et sur le projet GRASP-AGAIN (« Développement d’une neuroprothèse de préhension embarquée pour restaurer des capacités de préhension en vie quotidienne après un AVC » ; Promoteur : CHU de Toulouse ; PI : David Gasq)

